|
| Испарение и конденсация |
Пленочное кипение |
Сверхтекучий гелий |
Эксперименты | События | Библиотека |
Испарение и конденсацияПленочное кипениеСверхтекучий гелийЭксперименты События и мероприятияБиблиотека• История холода• Элементы физической кинетики• Разделение газовых смесей• Методические указания. Анализ криогенных установок• Оборудование гелиевого ожижителя Г-45• Методические указания. К практическим занятиям в криоцентре• Криогенные трубопроводы• Хранение и транпорт ожиженных газов• Основы методики проектирования криогенных установок• Вспомогательное оборудование криогенных установок• Расчет и оптимизация схем криогенных установок• Расчет низкотемпературных установок• Методика расчета схем криогенных установок (рефрижераторы и ожижители)• Методика расчета схем криогенных установок (рефрижераторы с нестационарными потоками)• Характеристики криогенных систем при работе на смесях• Механические свойства твердых тел при низких температурах• Людвиг Больцман. Лекции по теории газовСправочные данные БольцманиадаХейке Камерлинг-ОннесКриогениус |
Бродянский В.М. От твердой воды до жидкого гелия (история холода)5.3. СЕМЕЙСТВО "ЛЕНИВЫХ" ГАЗОВ ВЫХОДИТ В СВЕТОткрытие в воздухе инертных газов и исследование их уникальных свойств - заслуга английского физика У. Рамзая (1852-1916 гг.), который совместно с Дж. Рэлеем в 1894 г. открыл аргон, в 1895 г. обнаружил гелий на земле, а в 1898 г. совместно с М. Траверсом открыл криптон, ксенон и неон. В 1904 г. за эти открытия и определение места инертных газов в таблице Менделеева он был награжден Нобелевской премией. Отдавая должное заслугам Рамзая, не следует забывать; что первым обнаружил присутствие в воздухе примеси газов, не вступающих в химические реакции, другой великий физик - член Королевского общества Г. Кавендиш (1731-1810 гг.). Это открытие (как и многие другие) он не опубликовал, и оно стало известно из записей, найденных среди его бумаг намного позже. Известно, что Кавендиш работал в своей лаборатории один, Пользуясь только помощью слуги, выполнявшего по совместительству роль ассистента, не имея в своем распоряжении ни криогенной техники, ни спектрального анализа. И тем не менее он не только обнаружил инертные газы, но и определил их суммарное содержание в воздухе с погрешностью всего 9%. Ранее, в 1772 г., он открыл азот и изучил некоторые его свойства, но результат не опубликовал; поэтому честь открытия была отдана Л. Резерфорду, который сделал это в том же году, но позже. Именно знание химических свойств азота (открытых им самим) дало Кавендишу возможность обнаружить инертные газы. Пропуская через воздух, смешанный с кислородом, электрические разряды в присутствии воды, он установил, что при этом образуется азотная кислота. Поглощая ее едким калием КОН, он делал это до тех пор, пока объем газа не перестал уменьшаться (т.е. весь азот окислялся, а оксид был удален). Процесс химического связывания азота был длительным очень трудоемким, особенно для слуги Кавендиша, который во все время опыта крутил вручную электростатическую машину. После этого Кавендиш удалил оставшийся кислород и установил, что объем несконденсировавшегося газа составляет около 1/120 первоначального объема. Это и были инертные газы (по современным данным их содержание 1/109!). У. Рамзай уже через столетие не только вновь установил наличие в воздухе инертных газов, но и постепенно "вытащил" из смеси каждый по отдельности и изучил их свойства. Дело началось с того, что он и Рэлей заметили, что азот, получаемый из воздуха, тяжелее, чем полученный химическим путем. Разница и объяснялась содержанием инертных газов. Извлечение из воздуха каждого члена этого семейства и изучение их свойств было чрезвычайно трудной задачей, прежде всего потому, что их процентное содержание (кроме аргона) ничтожно (табл. 5.1). Какие эмоции у исследователей вызывала работа с этими как их тогда называли "благородными" газами, показывают названия, которые дал им крестный отец - Рамзай. Имена все греческие и поэтому для людей, не знающих этого языка, звучат вполне благозвучно. Однако аргон - "ленивый", криптон -"скрытый" (от этого же корня зашифрованная запись - "криптограмма"), ксенон - "чуждый". Такая вот газовая семейка. Только два газа, принадлежащие к ней, неон - "новый" и гелий - "солнечный", получили приятные имена. К. Линде, Ж. Клод и другие много работали над извлечением этих газов из воздуха. Подробное изложение связанных с этим интересных событий заняло бы слишком много места. Отметим только самое главное. Таблица 5.1. Содержание в воздухе и нормальные температуры кипения инертных газов
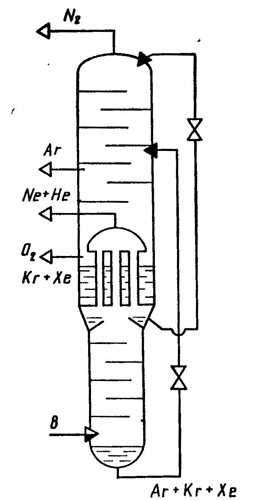
Еще в начале века было обнаружено, что во многих месторождениях природного горючего газа, добываемого в США и Канаде, содержится значительное количество гелия (до нескольких процентов). В дальнейшем такие газы были обнаружены и в других странах, поэтому вопрос о получении гелия из воздуха, где его содержание ничтожно, отпал сразу. В конце первой мировой войны в США были построены фирмами "Линде" и "Air Liquid" первые заводы по извлечению гелия из природного газа. Все остальные - аргон, неон, криптон и ксенон добываются только из воздуха одновременно с кислородом и азотом. Принципиальная основа этих процессов извлечения инертных газов становится ясной, если рассмотреть их поведение в колонне Линде двойной ректификации воздуха (рис. 5.14). Поступая с ожиженным воздухом В в нижнюю колонну совместно, они сразу же начинают вести себя по-разному - в соответствии со своими свойствами. Гелий и неон при температурах, существующих в колонне, остаются в газообразном состоянии; их температура конденсации намного ниже, чем у жидких кислорода и азота. Растворимость их в этих жидкостях ничтожна. Поэтому естественно, что гелий и неон вместе с парами поднимаются вверх по колонне и попадают в конденсатор. Здесь азот конденсируется и стекает вниз, а смесь неона и гелия остается газообразной и (хотя и медленно) накапливается под крышкой этого теплообменного аппарата. Отсюда ее можно (естественно, не в чистом виде, а в смеси с азотом) периодически отбирать для дальнейшего разделения и очистки. Количество ее по отношению к кислороду и азоту очень мало: на 1000 м3 переработанного воздуха выделяется 18,2 л неона и 5,2 л гелия. Из этой смеси, в которой неона примерно в 3 раза больше, чем гелия, его и выделяют.
Криптон и ксенон (тяжелые инертные газы), в отличие от гелия и неона, сразу переходят в жидкое состояние и растворяются в ожижаемом воздухе. Вместе с ним они попадают в испаритель нижней колонны, затем в верхнюю колонну и, наконец, собираются в жидком кислороде. Если из установки отбирается жидкий кислород, они уходят вместе с жидкостью, если газообразный, то с ним — другого пути нет. Содержание и криптона, и ксенона в кислороде в 5 раз больше, чем в воздухе (так как его получается в 5 раз меньше). Но и это количество ничтожно — в 1000 м3 кислорода содержится 5,7 л криптона и 4,3 см3 ксенона. Поэтому задачу извлечения Kr + Xe из кислорода можно было решать только на крупной промышленной установке, способной "переварить" большие количества кислорода, и постепенно, шаг за шагом, концентрировать эти "скрытый и чуждый" газы. Вместе с ними концентрировались в кислороде и другие, в том числе взрывчатые примеси воздуха (например, углеводороды), на которые сначала не обращали внимания — ведь содержание их было ничтожным. П. Рибо, сотрудник Ж. Клода, погиб при взрыве такой смеси, образовавшейся при опытах по концентрированию криптона и ксенона. Только в 20-е годы эту задачу удалось решить — криптон и ксенон стали обычными техническими продуктами (хотя и относительно дорогими). Что касается аргона, то его поведение в ректификационной колонне более сложно, чем остальных инертных газов. Поскольку гелий и неон — "легкокипящие", а криптон и ксенон — ,,тяжелокипящие", их положение в колонне четко определено: первые с паром идут вверх, вторые — с жидкостью вниз. Аргон же, как "среднекипящий", оказывается в трудном положении. Его температура кипения на 3K ниже, чем у кислорода, но на 10K выше, чем у азота. В нижней колонне, где нет полного разделения, он присоединяется к смеси, содержащей больше кислорода, попадает в испаритель и подается с жидкостью в верхнюю колонну. Тут уже производится окончательное разделение: надо выбирать, куда идти — вверх с азотом или вниз с кислородом. Но аргон оказывается в трудном положении: сверху на него льется холодный азот, который его конденсирует и смывает вниз, а снизу его подогревает более теплый кислородный пар, стремящийся вверх. У "ленивого" аргона, если его не отводить из середины колонны, остается один способ уйти — часть его выходит с кислородом, а другая часть — с азотом. В установках, где получают только кислород и азот, так и происходит. Такая ситуация и определяет способ извлечения аргона — его отводят из средней части верхней колонны, естественно, с неизбежными примесями кислорода и азота. Цель всей дальнейшей технологической цепочки сводится к получению чистого аргона путем удаления и кислорода, и азота. И К. Линде, и Ж. Клоду, каждому в своем варианте, удалось разработать такие технологии. Удаление азота и части кислорода производилось ректификацией, а окончательная очистка от кислорода — химическим путем — взаимодействием с серой или с водородом. В дальнейшем, уже в наше время, удалось достигнуть достаточно полной очистки аргона как ректификацией, так и адсорбцией. Первые соображения об использовании инертных газов высказывались еще в начале века (например, для заполнения газосветных трубок и электрических ламп накаливания), но широкое их применение развилось уже позже, в наше время. Таким образом, в классический период развития криогеники, закончившийся в начале ХХ в., были заложены основы как теории, так и криогенной техники. На этом фундаменте выросли целые направления техники и технологии со своей научной базой, обеспечившие существенный вклад в современную научно-техническую революцию. Параллельно с криогеникой бурно развивалась и холодильная техника. Она тоже вышла в первые годы ХХ в. с солидным научно-техническим заделом и производственным опытом. Более того, опередив криогенику в части практического использования своих возможностей, она раньше вышла на уровень возникновения и развития соответствующих новых технологий. При этом, естественно, продолжали совершенствоваться как сама холодильная техника, так и ее научная база. Обе последующие главы книги и посвящены развитию холодильного и криогенного направлений низкотемпературной науки, техники и технологии в эпоху подготовки и начала современной научно-технической революции. Следующая страница: 6. 1. Холодильная техника совершенствуется
|
|
Испарение и конденсация
Пленочное кипение
Сверхтекучий гелий
Эксперименты События Библиотека Справочники Больцманиада Камерлинг-Оннес Криогениус |
|
© Криофизика.рф 2006-2021. Молекулярно-кинетическая теория. Научные публикации. Испарение и конденсация. Плёночное кипение. Сверхтекучий гелий. |
о проекте условия использования |
контакты карта сайта |